Đề thi thử THPT quốc gia môn Hóa - THPT Thanh Chương 1 năm 2015Đề thi thử THPT quốc gia môn Hóa - THPT Thanh Chương 1 - Nghệ An năm 2015, các em tham khảo dưới đây:
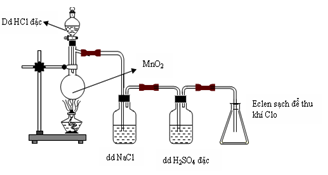
Câu 1: X là hỗn hợp 2 anđehit phân tử hơn kém nhau 1 nguyên tử Cacbon, không phải là đồng đẳng của nhau . Cho m gam X tác dụng tối đa với 0,4 mol H2 tạo ra hỗn hợp hai ancol Y. Cho Y tác dụng với Na dư thu được 0,2 mol H2. Mặt khác nếu cho m gam X tráng gương hoàn toàn thì thu được tối đa 129,6 gam Ag. Giá trị của m là A. 17,6 B. 1,76 C. 11,8 D. 1,18 Câu 2: Phản ứng nào dưới đây không phải là phản ứng oxi hóa – khử ? A. 2KI + H2O + O3 à 2KOH + I2 + O2 B. Cl2 + 2NaOH à NaCl + NaClO + H2O. C. 2H2S + SO2 à3S + 2H2O D. FeS + 2HCl à FeCl2 + H2S Câu 3: Để bó bột, đúc tượng người ta dùng A. CaSO4 B. CaCO3. C. CaSO4.H2O D. CaSO4.2H2O Câu 4: Hỗn hợp M gồm 1 peptit X và 1 peptit Y với tỷ lệ mol tương ứng là 1 : 2. Tổng số liên kết peptit trong 2 phân tử X và Y là 7. Thủy phân hoàn toàn m gam M thu được 60 gam glixin và 53,4 gam alanin. Giá trị m là A. 103,5g B. 113,4g C. 91g D. 93,6g Câu 5: Oxi hóa 4,6 gam etanol bằng CuO nung nóng được hỗn hợp X gồm andehit, ancol dư và nước. Biết hiệu suất phản ứng là 80%. Cho X tác dụng với Na dư thì thể tích H2 (đktc) thu được là A. 1,12 B. 0,448 C. 11,2 D. 4,48 Câu 6: Phát biểu nào sau đây là đúng ? A. Các kim loại kiềm thổ có cấu trúc mạng tinh thể lập phương tâm diện. B. Các kim loại kiềm thổ có độ cứng cao. C. Các nguyên tố có cấu hình electron lớp ngoài cùng là ns2 đều là kim loại kiềm thổ. D. Nhiệt độ nóng chảy, nhiệt độ sôi và khối lượng riêng của các kim loại kiềm thổ biến đổi không theo một quy luật nhất định. Câu 7: Có 3 dung dịch pH như nhau là HCl, H2SO4, H3PO4. Giả sử H2SO4 điện li hoàn toàn cả 2 nấc. Để trung hòa cùng thể tích từng dung dịch trên cần dùng lần lượt các dung dịch NaOH 1M với thể tích tương ứng là V1, V2, V3 lít. So sánh nào sau đây là đúng : A. V1 < V2 < V3 B. V1 = V2 < V3 C. V1 = 2V2 = 3V3 D. V1 = V2 = V3 Câu 8: Este X 3 chức ( không có nhóm chức nào khác ). Xà phòng hóa hoàn toàn 2,4 gam X bằng NaOH được chất hữu cơ Y không nhánh, dễ bay hơi và 2,7 gam hỗn hợp 3 muối của 1 axit cacboxylic no, đơn chức, mạch hở và 2 axit cacboxylic không nhánh đồng đẳng kế tiếp trong dãy đồng đẳng của axit acrylic . Chuyển toàn bộ hỗn hợp muối thành các axit tương ứng rồi đốt cháy hỗn hợp axit đó thu được 4,6 gam hỗn hợp CO2 và H2O. Đốt cháy hoàn toàn 2,4 gam X thu được tổng khối lượng nước và CO2 là A. 6,10g B. 5,92g C. 5,04g D. 5,22g Câu 9: Cho 300ml dung dịch (NH4)2SO4 1M tác dụng với 200 ml dung dịch Ba(OH)2 1M được dung dịch X. Cô cạn X được số gam chất rắn khan là A. 13,2 B. 59,8 C. 73,8 D. 46,6 Câu 10: Nung butan ở nhiệt độ cao với xúc tác thích hợp được hỗn hợp X gồm CH4, C2H6, C2H4, C3H6 và C4H10. Đốt cháy hoàn toàn 1/2 hỗn hợp X được 35,2 gam CO2 . Cho ½ hỗn hợp X còn lại vào dung dịch Brom dư thấy có 24 gam brom phản ứng. Hiệu suất phản ứng nung butan là A. 66,67% B. 50% C. 75% D. 80%. Câu 11: Công thức của 1 ancol no mạch hở là CnHm(OH)2. Mối quan hệ của m và n là A. m = n B. m = n + 2 C. m = 2n + 1. D. m = 2n Câu 12: Polime nào sau đây không phải là thành phần chính của chất dẻo A. Poli acrilonitrin B. Poli stiren. C. Poli (metyl metacrylat) D. Polietilen Câu 13: Các hợp kim Fe – Cu, Fe – Ag, Fe – C, Al-Fe tiếp xúc với không khí ẩm, trường hợp Fe bị ăn mòn nhanh nhất là A. Fe-C B. Fe-Ag C. Al-Fe D. Fe-Cu Câu 14: Kim loại nào không tác dụng với H2O ở nhiệt độ thường A. Ba B. Be C. Ca D. Na Câu 15: Phân tử nào sau đây có liên kết ion A. NaBr B. H2O C. NH3. D. HCl Câu 16: Cho Hình vẽ mô tả sự điều chế Clo trong phòng Thí nghiệm như sau:
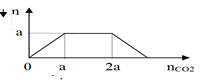
Phát biểu nào sau đây không đúng: A. Không thể thay dung dịch HCl bằng dung dịch NaCl. B. Có thể thay MnO2 bằng KMnO4 hoặc KClO3 C. Dung dịch H2SO4 đặc có vai trò hút nước, có thể thay H2SO4 bằng CaO. D. Khí Clo thu được trong bình nón là khí Clo khô. Câu 17: Để làm khô CO2 người ta dẫn khí CO2 có lẫn hơi nước đi qua A. Ca(OH)2 B. P2O5 C. NaOH đặc. D. CaO Câu 18: Hòa tan 13,7 gam Ba kim loại vào 100ml dung dịch CuSO4 1M được m gam kết tủa. Giá trị của m là A. 33,1 B. 23,3 C. 9,8 D. 6,4. Câu 19: Cho 0,02 mol Glyxin tác dụng với 300ml dung dịch HCl 1M được dung dịch X. Để tác dụng hết với các chất trong X cần vừa đủ V lít dung dịch NaOH 1M được dung dịch Y. Cô cạn cẩn thận Y được m gam chất rắn khan. Giá trị V và m là A. 0,32 và 23,45 B. 0,02 và 19,05 C. 0,32 và 19,05 D. 0,32 và 19,49 Câu 20: Cho 1,36 gam hỗn hợp X gồm Fe và Mg vào 400ml dung dịch CuSO4. Sau khi phản ứng xong thu được 1,84 gam chất rắn Y và dung dịch Z. Thêm NaOH dư vào Z được kết tủa. Nung kết tủa ngoài không khí đến khối lượng không đổi được 1,2 gam chất rắn. Nồng độ mol/l của dung dịch CuSO4 ban đầu là A. 0,02 B. 0,04 C. 0,05 D. 0,025 Câu 21: Hỗn hợp X gồm C2H2, C3H6, C4H10 và H2. Cho 11,2 lít (đktc) hỗn hợp X qua bình đựng dung dịch brom dư thấy có 64 gam brom tham gia phản ứng. Mặt khác, đốt cháy hoàn toàn 11,2 lít (đktc) hỗn hợp X được 55gam CO2 và m gam nước. Giá trị của m là A. 31,5 B. 27 C. 24,3 D. 22,5 Câu 22: Phát biểu nào sau đây là sai A. Dầu thực vật và mỡ động vật đều là chất béo. B. Tristearin có CTPT là C54H110O6 C. Dầu thực vật là chất béo thành phần có nhiều gốc axit béo không no nên ở thể lỏng. D. Phản ứng xà phòng hóa chất béo là phản ứng 1 chiều, xảy ra chậm. Câu 23: Nguyên tử của nguyên tố R có tổng số electron trên các phân lớp s bằng 5. R là A. Fe( Z = 26) B. Na ( Z =11) C. Al ( Z = 13) D. K ( Z = 19 ) Câu 24: Hòa tan hoàn toàn 28 gam hỗn hợp FeS2 và Cu2S có số mol bằng nhau trong dung dịch HNO3 đặc nóng được sản phẩm khử duy nhất là NO2 và dung dịch X. Số mol HNO3 đã phản ứng là ( toàn bộ S trong hợp chất ban đầu đều tạo thành SO42-) A. 2,6 B. 2,8 C. 3,0 D. 2,5 Câu 25: Cho cân bằng: X (k) + 3Y (k) 2Z (k). Khi tăng nhiệt độ thì tỉ khối của hỗn hợp khí so với H2 giảm đi. Phát biểu đúng khi nói về cân bằng này là A. Phản ứng nghịch tỏa nhiệt, cân bằng dịch chuyển theo chiều thuận khi tăng nhiệt độ. B. Phản ứng nghịch thu nhiệt, cân bằng dịch chuyển theo chiều thuận khi tăng nhiệt độ. C. Phản ứng thuận thu nhiệt, cân bằng dịch chuyển theo chiều nghịch khi tăng nhiệt độ. D. Phản ứng thuận tỏa nhiệt, cân bằng dịch chuyển theo chiều nghịch khi tăng nhiệt độ. Câu 26: Từ 12 kg quặng pirit chứa 80% FeS2, còn lại là tạp chất trơ có thể điều chế được bao nhiêu lít H2SO4 1M ( hiệu suất cả quá trình là 80%) A. 12,8 B. 128 C. 200 D. 160 Câu 27: Cho 5g kẽm viên vào cốc đựng 50ml dung dịch H2SO4 4M ở nhiệt độ thường (25°C). Trường hợp nào tốc độ phản ứng không đổi so với thí nghiệm trên ? A. Thay 5g kẽm viên bằng 5g kẽm bột. B. Dùng 100 ml dung dịch H2SO4 4M C. Thay 50 ml dung dịch H2SO4 4M bằng 100 ml dung dịch H2SO4 2M D. Thực hiện phản ứng ở 50°C Câu 28: Chất nào sau đây khi thủy phân tạo các chất đều có phản ứng tráng gương A. HCOOCH=CH2 B. HCOOCH3 C. CH3COOCH3 D. CH3COOCH=CH2 Câu 29: Cho dung dịch HCl tác dụng lần lượt với các dung dịch sau : Fe(NO3)2, NaF, NaOH, FeCl2, Na3PO4, CuSO4, AgNO3, số phản ứng xảy ra là A. 3 B. 6 C. 4 D. 5 Câu 30: Axit cacboxylic nào dưới đây là axit đơn chức A. Axit adipic B. Axit terephtalic. C. Axit oleic D. axit oxalic Câu 31: Phát biểu nào sau đây là đúng A. Các amino axit có số nhóm NH2 lẻ thì khối lượng phân tử là số chẵn. B. Các dung dịch : Glyxin, Alanin, Lysin đều không làm đổi màu quỳ. C. Amino axit đều là chất rắn kết tinh ở điều kiện thường. D. Amino axit độc. Câu 32: X là dung dịch chứa NaOH và 0,1 mol Ba(OH)2. Sục từ từ CO2 vào X, lượng kết tủa tạo thành được mô tả trong đồ thị dưới đây:
Số mol NaOH ban đầu là A. 0,2 B. 0,1 C. 0,3 D. 0,4 Câu 33: Cho các dung dịch : NaOH, Ba(HCO3)2, Ca(OH)2, HCl, NaHCO3, BaCl2 phản ứng với nhau từng đôi một. Số cặp chất xảy ra phản ứng ( nhiệt độ thường ) là A. 9 B. 8 C. 6 D. 7 Câu 34: Có bao nhiêu đipeptit có CTPT C6H12N2O3 ? A. 5 B. 3 C. 4 D. 6 Câu 35: Đun 17,1 gam hỗn hợp hai ancol M và N ( MM < MN) đồng đẳng kế tiếp với H2SO4 đặc ở 1700C được hỗn hợp anken X ( hiệu suất 100%). Để đốt cháy hoàn toàn X cần vừa đủ 30,24 lít oxi (đktc). Mặt khác, nếu đun 17,1 gam hỗn hợp ancol trên với H2SO4 ở 1400C thu được 10,86 gam hỗn hợp các ete. Biết hiệu suất tạo ete của M là 60%, hiệu suất tạo ete của N là A. 70% B. 63,5% C. 80% D. 75%. Câu 36: Chất X có công thức : CH3 – CH=CH-CH(OH)-CH3 có tên gọi là A. penten-2-ol B. pent-2-en-4-ol C. pent-2-en-2-ol. D. pent-3-en-2-ol. Câu 37: Chia 5,56 gam hỗn hợp X gồm Fe và 1 kim loại M có hóa trị không đổi thành 2 phần bằng nhau, phần 1 hòa tan hết trong dung dịch HCl thu được 1,568 lít H2. Phần 2 hòa tan hết trong dung dịch HNO3 loãng dư thu được 1,344 lít NO( sản phẩm khử duy nhất, đktc). Phần trăm theo khối lượng của M trong X là A. 19,42% B. 40,29% C. 80,58% D. 59,71% Câu 38: X là chất được dùng trong công nghiệp dược phẩm ( thuốc đau dạ dày…), trong công nghiệp thực phẩm ( bột nở…). X là A. Na2CO3 B. NH4HCO3 C. NH4Cl. D. NaHCO3 Câu 39: Ở điều kiện thường, X là chất rắn mùi sốc, dùng để tẩy uế, khử trùng, có khả năng tẩy màu. X là A. Nước gia ven B. O3. C. SO2 D. clorua vôi. Câu 40: Hỗn hợp X gồm ancol metylic và ancol M no đơn chức mạch hở.Cho 15,2 gam X tác dụng với Na dư thu được 3,36 lít H2 (đktc). Mặt khác oxi hóa hết 7,6 gam hỗn hợp X bằng CuO nung nóng rồi lấy sản phẩm cho tráng gương hoàn toàn thu được 21,6 gam Ag. CTCT thu gọn của M là A. CH3CH2CH2OH B. C2H5OH C. CH3CHOHCH3 D. CH3CHOHCH2CH3 Câu 41: X là hỗn hợp C3H6 và C4H10. Sục V lít X (đktc) vào dung dịch Brom dư thấy có 16 gam brom phản ứng. Mặt khác đốt cháy hoàn toàn V lít (đktc) như trên tạo ra 30,8 gam CO2 . Giá trị V là A. 6,72. B. 2,24 C. 4,48 D. 3,36 Câu 42: Hòa tan 33,8 gam oleum H2SO4.3SO3 vào 100g nước được dung dịch H2SO4 có nồng độ % là a. Giá trị của a là A. 22 B. 39,2 C. 29,3 D. 7,3 Câu 43: Để trung hòa 100ml dung dịch H2SO4 1M cần V ml NaOH 1M. Giá trị của V là A. 100 B. 150 C. 50 D. 200 Câu 44: Cho các chất KMnO4, KClO3, MnO2, K2MnO4 lấy cùng số mol tác dụng hoàn toàn với HCl dư, trường hợp tạo ít clo nhất A. K2MnO4 B. MnO2 C. KClO3 D. KMnO4 Câu 45: Dung dịch X chứa m gam hỗn hợp CuSO4 và NaCl. Thực hiện điện phân dung dịch X cho đến khi nước bắt đầu điện phân ở cả 2 điện cực thì dừng lại, khi đó ở anot thoát ra 4,48 lít khí (đktc). Dung dịch sau điện phân có thể hòa tan tối đa 2,7 gam Al. Giá trị lớn nhất của m là A. 47,4g B. 58,625g C. 55,4g D. 34,625g. Câu 46: Số hợp chất hữu cơ đơn chức chứa C, H, O, tác dụng với Na, có số nguyên tử cacbon trong phân tử không quá 2 là A. 4 B. 6 C. 2 D. 5 Câu 47: Cho các chất : phenol, stiren, benzen, toluen, anilin, triolein, glixerol. Số chất tác dụng được với nước Brom là A. 6 B. 5 C. 4 D. 3 Câu 48: Chất nào sau đây không tráng gương A. Axetilen B. Fructozơ C. Glucozơ D. fomandehit Câu 49: Chất không tham gia phản ứng thủy phân là A. Tinh bột B. Xenlulozơ C. Saccarozơ D. glucozơ Câu 50: Cho m gam một axit cacboxylic mạch không nhánh tác dụng với NaHCO3 dư được 2,24 lít CO2 (đktc). Mặt khác, cũng m gam axit trên tác dụng với Ca(OH)2 dư được 9,1 gam muối. X là A. axit fomic. B. axit axetic C. axit oxalic D. axit acrylic Đáp án sẽ được Tuyensinh247 cập nhật sau, các em chú ý theo dõi. Nguồn: Dethi.violet DÀNH CHO BẠN – LỘ TRÌNH LUYỆN THI TỐT NGHIỆP THPT - ĐGNL - ĐGTD!
Xem ngay lộ trình luyện thi 3 trong 1 tại Tuyensinh247: Luyện thi TN THPT - ĐGNL - ĐGTD ngay trong 1 lộ trình.
Xem thêm thông tin khoá học & Nhận tư vấn miễn phí - TẠI ĐÂY
Xem thêm tại đây:
Đề thi thử tốt nghiệp THPT môn Hóa 2025
>> Lộ Trình Sun 2025 - 3IN1 - 1 lộ trình ôn 3 kì thi (Luyện thi TN THPT & ĐGNL; ĐGTD) tại Tuyensinh247.com. Đầy đủ theo 3 đầu sách, Thầy Cô giáo giỏi, 3 bước chi tiết: Nền tảng lớp 12; Luyện thi chuyên sâu; Luyện đề đủ dạng đáp ứng mọi kì thi.
|
|||||||||||||
-
Đề thi thử THPT quốc gia môn Hóa - THPT chuyên Hà Giang năm 2015
Đề thi thử THPT quốc gia môn Hóa - THPT chuyên Hà Giang năm 2015, các em tham khảo dưới đây:
-
Đề thi thử THPT quốc gia môn Hóa - THPT Cẩm Giàng II năm 2015
Đề thi thử THPT quốc gia môn Hóa - THPT Cẩm Giàng II Hải Dương năm 2015, các em tham khảo dưới đây:
-
Đề minh họa môn Anh kỳ thi V-SAT 2025 - Có đáp án
Đề thi minh họa kỳ thi đánh giá đầu vào V-SAT 2025 đã được công bố. Tham khảo ngay đề thi môn Tiếng Anh kèm hướng dẫn giải chi tiết được Tuyensinh247 đăng tải dưới đây.
-
Đáp án và Đề minh họa kỳ thi V-SAT 2025 môn Lí
Tham khảo đề thi minh họa và đáp án V-SAT 2025 kỳ thi đánh giá đầu vào (VSAT) môn Vật Lí được cập nhật dưới đây.
-
Đề minh họa môn Sinh kỳ thi V-SAT 2025
Xem ngay đề thi minh họa môn Sinh học kỳ thi đánh giá đầu vào V-SAT năm 2025 được đăng tải chi tiết bên dưới.